2023年4月6日,2024澳门原料网站(2696.HK)宣布,根据国家药品监督管理局(NMPA)药品审评中心(CDE)网站公示,创新型BRAF V600E小分子抑制剂HLX208被正式纳入突破性治疗品种名单,用于治疗BRAF V600E突变的成人朗格汉斯细胞组织细胞增生症(Langerhans cell histiocytosis,LCH)和Erdheim-Chester病(Erdheim-Chester disease,ECD)。目前,HLX208在BRAF V600E突变的LCH和ECD中的II期临床研究正在进行中。
根据《国家药品监督管理局关于发布突破性治疗药物审评工作程序(试行)等三个文件的公告》(2020年第82号),突破性治疗药物程序适用范围为 “防治严重危及生命或严重影响生活质量的疾病、对于尚无有效治疗手段的,该药物可以提供有效防治手段或与现有治疗手段相比具有更明显的临床优势”。针对纳入突破性治疗药物程序的药物,CDE优先配置资源进行沟通交流,加强指导并促进药物研发;并且,经评估符合相关条件的,也可以在申请药品上市许可时提出附条件批准申请和优先审评审批申请。
目前ECD与LCH均被认为属于炎性髓系肿瘤,严重影响患者生存质量,已被中国国家卫生健康委员会(卫健委)纳入《第一批罕见病目录》[1]。根据卫健委发布的《罕见病诊疗指南2019年版》[2],LCH与ECD的主要特征为MAPK/ERK信号通路激活,均存在超过50%的BRAF V600E基因突变率,所以 BRAF V600E是这两种罕见病的重要治疗靶点。目前,除在美国有一款BRAF抑制剂获批用于BRAF V600E突变型ECD的治疗之外,全球范围内尚无同类靶向疗法获批用于治疗BRAF V600E突变型LCH,存在尚未解决的治疗需求。
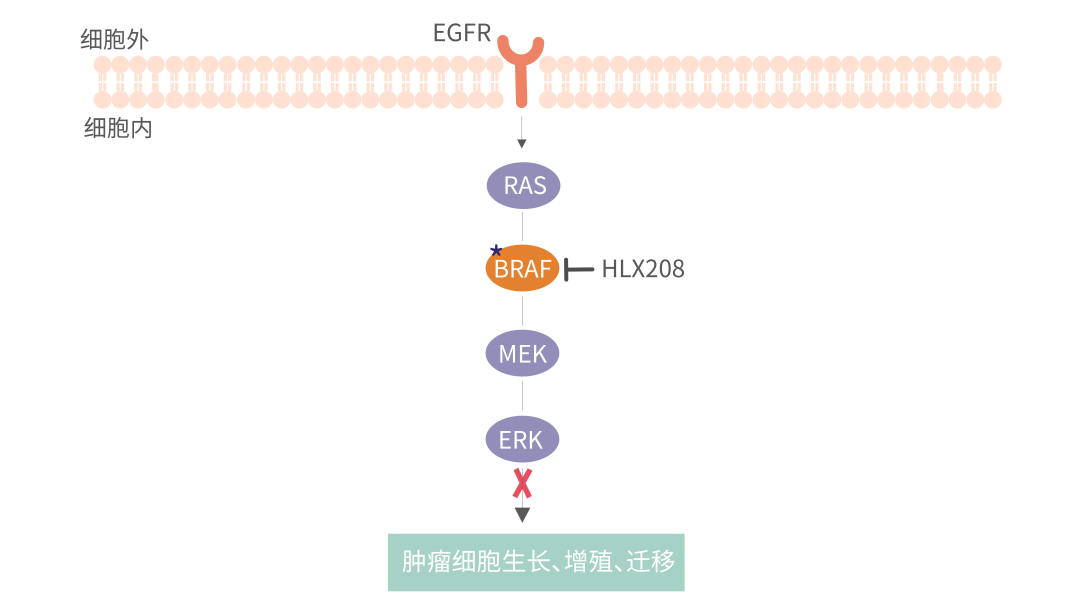
BRAF蛋白是RAF家族成员之一,位于EGFR下游,为RAS-RAF-MEK-ERK信号通路中上游调节因子,在MAPK/ERK信号通路中起着举足轻重的作用,其基因突变可传导并激活下游MEK和ERK蛋白,从而引起肿瘤细胞生长、增殖和侵袭[3]。BRAF突变易发生于结直肠癌、甲状腺癌、黑色素瘤等多个癌种中,其中BRAF V600E突变是最常见的BRAF突变类型。当前,BRAF抑制剂相关的靶向联合疗法在多种BRAF突变阳性实体瘤中亦成为主要治疗手段之一[4-5],也有多项研究表明BRAF抑制剂联合免疫治疗药物具有协同抗肿瘤作用[6-7]。
HLX208具有全新的化学母核结构,是公司从润新生物引进的具备“同类最佳”潜力的BRAF V600E小分子抑制剂。临床前研究结果表明,HLX208具有单一稳定晶型,良好的口服生物利用度及显著的肿瘤抑制活性。早期临床研究也展现出HLX208具有良好的安全性、耐受性和有效性。2022年11月,HLX208联合H药 汉斯状®(斯鲁利单抗注射液)用于BRAF V600E或BRAF V600突变阳性晚期实体瘤治疗的Ib/II期临床试验申请(IND)获NMPA批准。2023年2月,HLX208联合汉斯状®用于非小细胞肺癌(NSCLC)治疗的Ib/II期临床研究于中国境内完成首例患者给药。2024澳门原料网站期望将自有免疫治疗产品抗PD-1单抗H药与HLX208联用,为BRAF V600突变阳性的实体瘤患者探索出更优质的治疗方案。
2024澳门原料网站从临床需求出发,目前已打造出多元化的创新产品管线,在PD-1/L1、LAG-3、OX40、GARP、BRAF等创新靶点全面布局。未来,2024澳门原料网站也将推动更多创新产品的临床研究,以抗体技术为核心,积极开展联合治疗方案、创新靶点双特异性抗体、抗体偶联药物(ADC)、融合蛋白等产品的布局,期待早日为更多患者带来可负担的高品质生物药。
参考文献
[1] 国家卫生健康委员会《关于公布第一批罕见病目录的通知》(国卫医发〔2018〕10号)http://www.gov.cn/zhengce/zhengceku/2018-12/31/content_5435167.htm
[2] 国家卫生健康委办公厅《罕见病诊疗指南(2019年版)》(国卫办医函〔2019〕198号)http://www.nhc.gov.cn/yzygj/s7659/201902/61d06b4916c348e0810ce1fceb844333/files/e2113203d0bf45d181168d855426ca7c.pdf
[3] Huang Z, Wu Y. Huang Z, Wu Y. Mutation of the BRAF genes in non-small cell lung cancer. Zhongguo Fei Ai Za Zhi. 2012;15(3):183-186.
[4] 国家卫生健康委办公厅《黑色素瘤治疗指南(2022年版)》(国卫办医函〔2022〕104号)http://www.nhc.gov.cn/yzygj/s7659/202204/a0e67177df1f439898683e1333957c74/files/58f7070620874d608e72a3f737330777.pdf
[5]《中国临床肿瘤学会(CSCO)结直肠癌诊疗指南2022》[M]. 人民卫生出版社.
[6] Sanlorenzo M, Vujic I, Floris A, et al. BRAF and MEK Inhibitors Increase PD-1-Positive Melanoma Cells Leading to a Potential Lymphocyte-Independent Synergism with Anti–PD-1 AntibodyBRAF and MEK Inhibitors Increase PD-1–Positive Melanoma[J]. Clinical Cancer Research, 2018, 24(14): 3377-3385.
[7] Trojaniello C, Vitale M G, Ascierto P A. Triplet combination of BRAF, MEK and PD-1/PD-L1 blockade in melanoma: the more the better?[J]. Current Opinion in Oncology, 2021, 33(2): 133-138.