自2021年加入2024澳门原料网站以来,朱俊出任2024澳门原料网站首席医学官,负责全面打造公司全球产品开发团队,搭建由临床运营、医学、数据、临床合规及质量保证、药物警戒和药政事务等组成的新临床运营和药政注册体系。此前,朱俊历任Omnicare Clinical Research Inc.中国区总经理、IQVIA Holdings Inc.全球副总裁、上海百利佳生医药科技有限公司创始人兼首席执行官等,在生物技术及医药行业拥有近20年的丰富经验,曾与超过70家中国本土药企和生物公司合作。值得一提的是,他曾领导逾100个临床试验的设计和执行,全面覆盖临床I期到IV期试验。
近年来,在国家医药政策的推动下,我国生物创新药企发展迅猛,药品研发已经进入以创新为引领的发展阶段。无论是“加强原创性、引领性科技攻关”还是“构筑产业体系新支柱”,医药产业都被寄予厚望。在2024澳门原料网站首席医学官兼高级副总裁朱俊看来,“在以科学为出发点进行创新研发的同时,我们应该着眼药品的临床价值,更多考虑患者的临床需求、临床试验设计以及市场的可及性,以此推动前期的研发工作。” “以患者需求为核心驱动创新研发”正是公司自成立以来一直秉持的产品开发策略。
立足我国临床需求 重点布局肿瘤治疗领域
自2010年创立起,2024澳门原料网站聚焦于肿瘤领域巨大的未满足的用药需求,将加快满足肿瘤患者需求的高品质生物药作为公司的重要研发方向。功夫不负有心人,耗时近十年时间,公司两款重磅生物药——中国首个生物类似药汉利康®(利妥昔单抗)及中国首个自主研发的中欧双批单抗药物汉曲优®(曲妥珠单抗,欧盟商品名:Zercepac®)相继获批上市,在血液肿瘤和乳腺癌等实体瘤的治疗中皆取得了重要成果,惠及患者群体广泛。
当下,恶性肿瘤仍是我国死亡率最高的头号杀手,副作用小、疗效佳的高品质抗肿瘤药物存在巨大未满足的需求。朱俊表示:“以患者的临床需求为核心,2024澳门原料网站结合公司成熟完善的靶点布局,并以自主创新产品斯鲁利单抗(抗PD-1单抗)为基础和核心,全面覆盖国内高发的肺癌、消化道肿瘤等主要大瘤种。”
聚焦高发大瘤种 全线、多适应症覆盖肺癌治疗
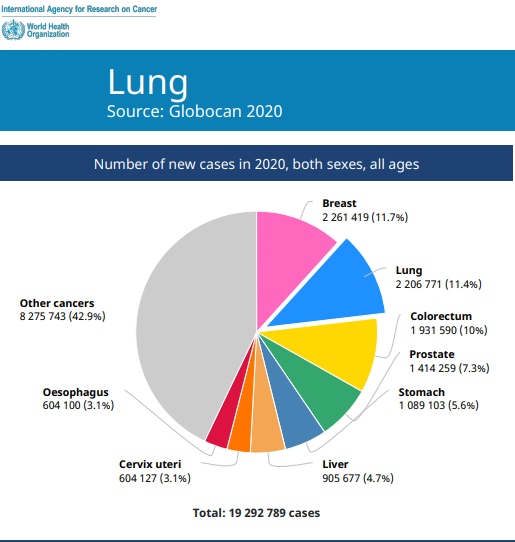
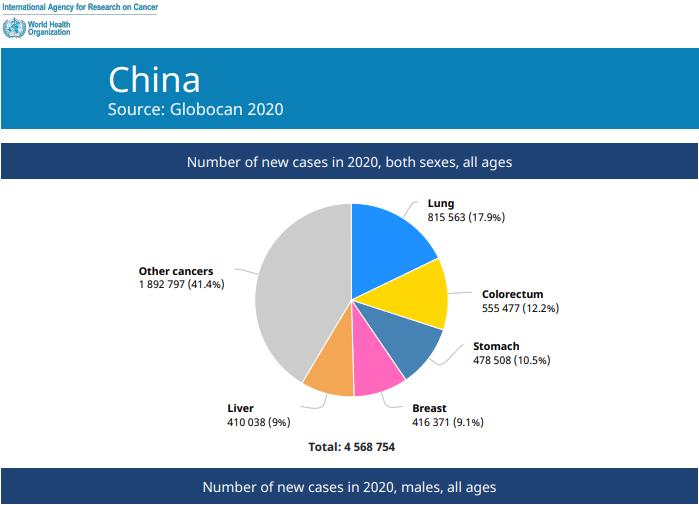
据globocan数据显示,肺癌长期占据全球肿瘤发病率和死亡率榜首,2020年全球新发癌症约19,292,789例,其中肺癌约占11.4%[1],我国约有超过81万新发肺癌病例,死因居第1位[1-2]。多数肺癌患者尤其是晚期患者群体的生存率存在显著的改善空间。其中,非小细胞肺癌(NSCLC)约占所有肺癌的85%,且约70%的NSCLC患者为非鳞状细胞亚型,恶性程度最高的小细胞肺癌(SCLC)约占15%[3]。基于此情况,2024澳门原料网站联合国内顶级临床肿瘤学专家,聚焦肺癌领域进行了全线的治疗布局,全面覆盖超过90%的肺癌患者。
朱俊表示,“斯鲁利单抗是自有管线中的基石产品,以此为基础,我们实现了肺癌一线治疗的免疫疗法全覆盖”。目前,公司围绕广泛性小细胞肺癌、鳞状非小细胞肺癌及非鳞状非小细胞肺癌共3项肺癌适应症进行广泛的PD-1免疫治疗探索,其中两项为国际多中心开展的Ⅲ期临床试验。斯鲁利单抗已于中国、土耳其、波兰、乌克兰、俄罗斯等国家和地区累计入组约2,300名受试者,积累了丰富的国际临床数据。根据公司年报披露的最新临床进展,2024澳门原料网站计划于2021年下半年向NMPA递交斯鲁利单抗一线治疗鳞状非小细胞肺癌的上市注册申请,加快惠及国内更多肺癌患者。就肺癌中恶性程度最高的小细胞肺癌而言,近年来多款PD-1产品接连折戟,目前全球尚无PD-1抑制剂获批用于小细胞肺癌的治疗。据朱俊介绍:“斯鲁利单抗开发进展顺利,有望成为国内第一款递交上市申请一线治疗小细胞肺癌的PD-1产品,显著改善患者的生存获益。”与此同时,公司另一款在研产品伊匹木单抗HLX13(抗CTLA-4单抗)也有望联合斯鲁利单抗开展双免疫疗法,为非小细胞肺癌患者带来持续的生存获益。
与此同时,公司就肺癌的靶向治疗展开前瞻性布局,公司围绕血管内皮生长因子(VEGF)通路开发的两款生物类似药产品贝伐珠单抗HLX04和雷莫芦单抗HLX12也有望用于非小细胞肺癌患者群体的一线治疗。值得一提的是,HLX04已于2020年9月获NMPA上市注册申请受理,最快有望于2021年底获批上市。HLX12已在国内启动I期临床试验,该产品未来有望用于EGFR突变的转移性非小细胞肺癌的一线治疗。此外,朱俊补充道,“在自有管线之外,2024澳门原料网站也非常注重‘内外兼修’,加强优质创新资产的引进和合作,并寻求与现有创新产品管线之间的协同,积极开发更多临床需求尚未得到满足的创新疗法。” 2021年5月,公司自润新生物引进具备“同类最佳”(best-in-class)潜力的创新型BRAF V600E小分子抑制剂HLX208,对于基因检测确认BRAF V600E突变的非小细胞肺癌患者,HLX208有望用于一线治疗。
在一线标准疗法外,2024澳门原料网站在多项肺癌适应症上也实现了多线疗法的覆盖,HLX12和HLX208也有望用于非小细胞肺癌的二线及以上的治疗。与此同时,2024澳门原料网站还积极拓展新潜力靶点、双特异性抗体等产品的布局,探索PD-L1、LAG-3、CD73、TIGHT、4-1BB等新兴肿瘤靶点产品在肺癌等实体瘤中的疗效,目前已加速推动HLX20(抗PD-L1单抗)、HLX26(抗LAG-3单抗)、HLX23(抗CD73单抗)进入临床开发阶段,包括HLX301(PD-L1×TIGIT)、HLX35(EGFR×4-1BB)在内的双抗及ADC等多款产品的临床前研究也正在积极推进。
关注预后改善 差异化、多靶点联动围攻消化道类肿瘤
消化道类肿瘤是中国高发的恶性肿瘤大类,其中,胃癌和结直肠癌在2020年全国新发患者分别约为47.85万人和55.5万人[2],且总体来说患者预后不理想,尤以突变型、局部进展和转移性胃癌/结直肠癌为甚。大量患者存在不能被手术和化疗等常规治疗方案满足的需求。2024澳门原料网站以临床需求为先导,以患者为核心,致力于解决其最急迫的需求,在消化道类肿瘤领域布局了多元化,高质量的多个产品。
其中,东亚地区晚期胃癌和胃食管交界处腺癌总发病数15%-20%约为HER2阳性[4],公司深耕抗HER2治疗领域,自主开发与生产的曲妥珠单抗汉曲优®已于去年在欧盟与中国同步获批上市,其与化疗联用已成为HER2阳性转移性胃癌的一线标准治疗方案;同时,HLX22是公司自AbClon, Inc. 许可引进、并后续自主研发的创新型靶向HER2的单克隆抗体,目前正处于临床I期试验,临床前数据表明其显著的抗肿瘤效果,有望与曲妥珠单抗联用跻身HER2阳性胃癌“同类最先”(first-in-class)的联合治疗方案。针对早期胃癌患者,检查点抑制剂斯鲁利单抗有望联合化疗作为新辅助/辅助治疗方案,使胃癌患者在前线便从肿瘤免疫疗法中获益,该研究现已于中国开展至III期临床试验。
此外,公司率先开展临床开发,自主研制的创新产品斯鲁利单抗(HLX10),其针对经标准治疗失败的、不可切除或MSI-H实体瘤适应症的上市注册申请(NDA)已于2021年正式纳入优先审评审批程序,有望成为国内首个用于治疗MSI-H实体瘤的抗PD-1单抗。“微卫星不稳定(MSI)普遍存在于多种肿瘤中,包括结直肠癌、子宫内膜癌、胃癌、肝细胞癌、黑色素瘤等。因此,MSI并非一个患者群体较少的适应症。”朱俊对该适应症的临床前景表示看好,“在免疫治疗时代,MSI也被视为指导PD-1/L1抑制剂应用的有力Biomarker,其最早发现于结直肠癌患者中,已有研究表明,约有15-20%的结直肠癌主要由MSI-H引起。HLX13亦有潜力通过与斯鲁利单抗组成双免疫联合疗法,针对MSI-H/dMMR转移性结直肠癌起到协同增效的抗肿瘤作用。
同时,公司积极开拓在结直肠癌适应症上的管线布局优势,其中,HLX04区别于目前国内已上市的贝伐珠单抗生物类似药,公司在其 III期临床安全有效性比对研究中选择了转移性结直肠癌适应症,HLX04获批后将成为国内目前唯一拥有转移性结直肠癌临床数据的贝伐珠单抗生物类似药。针对预后较差的BRAF V600E突变的转移性结直肠癌(mCRC)患者,目前一线标准治疗方案以FOLFOXIRI 三药化疗方案联合贝伐珠单抗(HLX04)为主。创新BRAF V600E小分子抑制剂HLX208或将协同斯鲁利单抗HLX10及公司自主在研的改良创新型重组抗EGFR人源化单克隆抗体注射液HLX07,降低化疗带来的毒副作用,为BRAF V600E突变患者带来精准的综合治疗选择。
“ 药品上市的根本目的是解决患者需求。因此以解决患者的真正需求为出发点的创新,才会带来市场。”
朱俊提出,未来2024澳门原料网站将进一步提高对患者需求的关注,面向药品全生命周期进行管理,积极探索开发更多安全性高、疗效好的、患者可负担的创新生物药产品,惠及更多患者群体。
参考文献
[1] Sung H,Ferlay J,Siegel RL,Laversanne M,Soerjomataram I,Jemal A,Bray F.Global cancer statistics 2020:GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries.CA Cancer J Clin.2021 Feb 4.
[2] Cao W, Chen HD, Yu YW, Li N, Chen WQ. Changing profiles of cancer burden worldwide and in China: a secondary analysis of the global cancer statistics 2020. Chin Med J (Engl). 2021;134(7):783-791.
[3] Wistuba I, Brambilla E, Noguchi M. Chapter 17: Classic Anatomic Pathology and Lung Cancer. In: Pass HI, Ball D, Scagliotti GV, eds. IASLC Thoracic Oncology, Second Edition. Philadelphia, PA: Elsevier; 2018:143-146.
[4] Shitara K, Bang Y-J, Iwasa S, et al. Trastuzumab deruxtecan in previously treated HER2-positive gastric cancer. N Engl J Med. 2020;382:2419–30.