2024年9月18日,復宏漢霖(2696.HK)宣布,首個創新型單抗 H藥 漢斯狀®(斯魯利單抗)、中美歐三地獲批的曲妥珠單抗生物類似藥漢曲優®的多項最新研究結果在2024歐洲腫瘤內科學會(ESMO)大會上以壁報形式展示。
H藥 漢斯狀®為復宏漢霖自主研發的重組人源化抗PD-1單抗注射液,也是全球首個獲批一線治療小細胞肺癌的抗PD-1單抗,已在中國、印尼、柬埔寨、泰國等地獲批上市。以臨床需求為導向,公司圍繞H藥進行了差異化、多維度的適應症布局,廣泛覆蓋肺癌、消化道腫瘤等高發大癌種。目前,H藥已獲批用於治療微衛星高度不穩定(MSI-H)實體瘤、鱗狀非小細胞肺癌(sqNSCLC)、廣泛期小細胞肺癌(ES-SCLC)和食管鱗狀細胞癌(ESCC)4項適應症,惠及患者約80,000人。其一線治療ES-SCLC的歐盟上市許可申請(MAA)已獲得歐洲藥品管理局 (EMA) 受理,有望於2024年獲批上市。此外,公司積極推進H藥在更多差異化適應症中的創新聯合療法,如H藥聯合貝伐珠單抗及化療一線治療轉移性結直腸癌(mCRC),聯合化療用於胃癌的新輔助/輔助治療,聯合化療同步放療治療局限期小細胞肺癌(LS-SCLC)等。
漢曲優®(曲妥珠單抗,美國商品名:HERCESSI™,歐洲商品名:Zercepac®)是復宏漢霖按照中國、歐盟和美國等生物類似藥法規自主研發的曲妥珠單抗,也是公司首個通過FDA批准在美國開展商業化的產品,可用於治療HER2陽性早期乳腺癌、轉移性乳腺癌和轉移性胃癌,涵蓋原研已獲批准的所有適應症。目前,漢曲優®已在全球48個國家和地區獲批上市,累計惠及210,000+患者,為全球乳腺癌和胃癌患者帶來可負擔、高品質的治療選擇。
本次ESMO大會上發布的研究數據結果如下:
ASTRUM-005

論文題目
ASTRUM-005小細胞肺癌患者中吸煙相關突變的探索性研究
試驗方法
試驗設計ASTRUM-005是一項針對廣泛期小細胞肺癌(ES-SCLC)患者開展的隨機、雙盲、安慰劑對照的國際多中心III期臨床試驗。
吸煙特徵分析
302名患者的基線腫瘤組織樣本經 Med1CDxTM panel進行高通量測序分析基因突變,包括601個基因的外顯子區。研究中利用兩種生物信息學方法,即分別通過計算顛轉(Transversion)和轉換(Transition)比率(Ratio),以及吸煙相關突變占比(Cosmic數據庫中Signature 4)來分析吸煙相關的基因突變特徵,並採用Wilcoxon檢驗計算不同吸煙史患者之間的差異。在此前的非小細胞患者的分析研究中,這兩種方法都可以觀測到不同吸煙史患者之間的顯著區別[1]。由於非吸煙的小細胞肺癌患者人數較少,之前未開展小細胞肺癌的相關研究。
TTR:使用Maftools計算每個樣本中顛轉(嘌呤置換嘧啶或嘧啶置換嘌呤的突變)及轉換(嘌呤間或嘧啶間的置換突變)的數量,並計算這兩種數量的比率(TTR值)。分析中包括了所有同義/非同義突變[2-3]
Signature 4:參考Cosmic數據庫中對於不同突變特徵的注釋[4],使用R軟件包deconstructSigs[5]提取各個樣本的突變特徵信息,並計算與吸煙相關突變特徵(Signature 4)對於所有突變的占比。
統計分析
無進展生存期(PFS)和總生存期(OS)的中位數由乘積限(Kaplan-Meier)估計法計算得出,其中 n 是每個亞組類別中的患者人數。風險比(HR)及其95%置信區間(CI)採用未分層的Cox比例風險回歸模型計算;並列關係使用Efron法處理。基因組的吸煙特徵分析,使用 Wilcoxon 檢驗來計算不同吸煙史患者之間的差異。臨床數據截止日期為2022年6月13日。
結果
吸煙組的基線特徵
SCLC隊列中的患者(N = 302)根據吸煙史進行分組;其 23%患者當前吸煙,55%患者曾經吸煙,22%患者從不吸煙。患者的基線特徵匯總如下。
當前/既往吸煙組和不吸煙組患者的突變分析表明,最常發生突變的基因為 TP53 (90%和 91%)、RB1(68%和 69%)和 LRP1B(31%和 28%)。突變基因的差異分析表明,吸煙者與非吸煙者在常見突變基因方面相似,不吸煙者的常見突變基因包括EGFR、DMD、 MED12、MTOR、NOTCH1、REL、PGR、DNMT1、GRM3、KMT2A 和 CD22 等。
SCLC 患者的吸煙特徵
兩種方法均未發現不同吸煙史組間的吸煙特徵存在明顯差異(TTR:P = 0.54;Sigature 4:P = 0.38)。
我們對既往研究中全外顯子組測序分析的兩個隊列數據集進行相同的分析,驗證了上述結果[1,6]。該研究中,來自 40 名 SCLC 患者的 120 份樣本顯示,無論採用哪種方法,都沒有觀察到突變模式與吸煙史之間的相關性。
在另一個獨立的數據集中,我們對 110 例 SCLC 患者樣本進行了全外顯子組測序(數據未公布)[7],也觀察到了相似的結果。根據 1.12 這一中位TTR值,我們將患者進一步分為高/低 TTR 組。突變分析表明,REL 在非吸煙者中突變頻率更高(P < 0.001)。
基於TTR值的分組,我們分析了不同組患者分的預後情況。對僅接受化療的患者而言,TTR越高,中位OS則越短(HR [95% CI], 1.65 [1.05-2.62]; P = 0.03)。而對斯魯利單抗聯合化療組的患者,高TTR和低TTR組間的臨床獲益相似(HR [95% CI],0.97 [0.67-1.4]; P = 0.87)。
無論TTR高低,兩個治療組(化療組和斯魯利單抗聯合化療組)的患者在PFS方面的獲益皆相似。(HR [95% CI], 1.25 [0.83-1.88]; P = 0.29 和 0.95 [0.67-1.34]; P = 0.77)。
結論
本臨床試驗ASTRUM-005中共有67名(22%)無吸煙史的SCLC患者。我們的研究表明,SCLC患者無論吸煙與否,都存在類似的吸煙相關基因組突變特徵,該發現與此前在NSCLC患者中的研究結果不同。這一研究結果提示,SCLC患者可能會發生與煙草直接接觸無關的其他來源的基因顛換突變;且生存分析顯示,高TTR的患者可能從化療中獲益較少,表明SCLC中的突變可以作為特定療法的預測性生物標誌物。
ASTRUM-004
論文題目
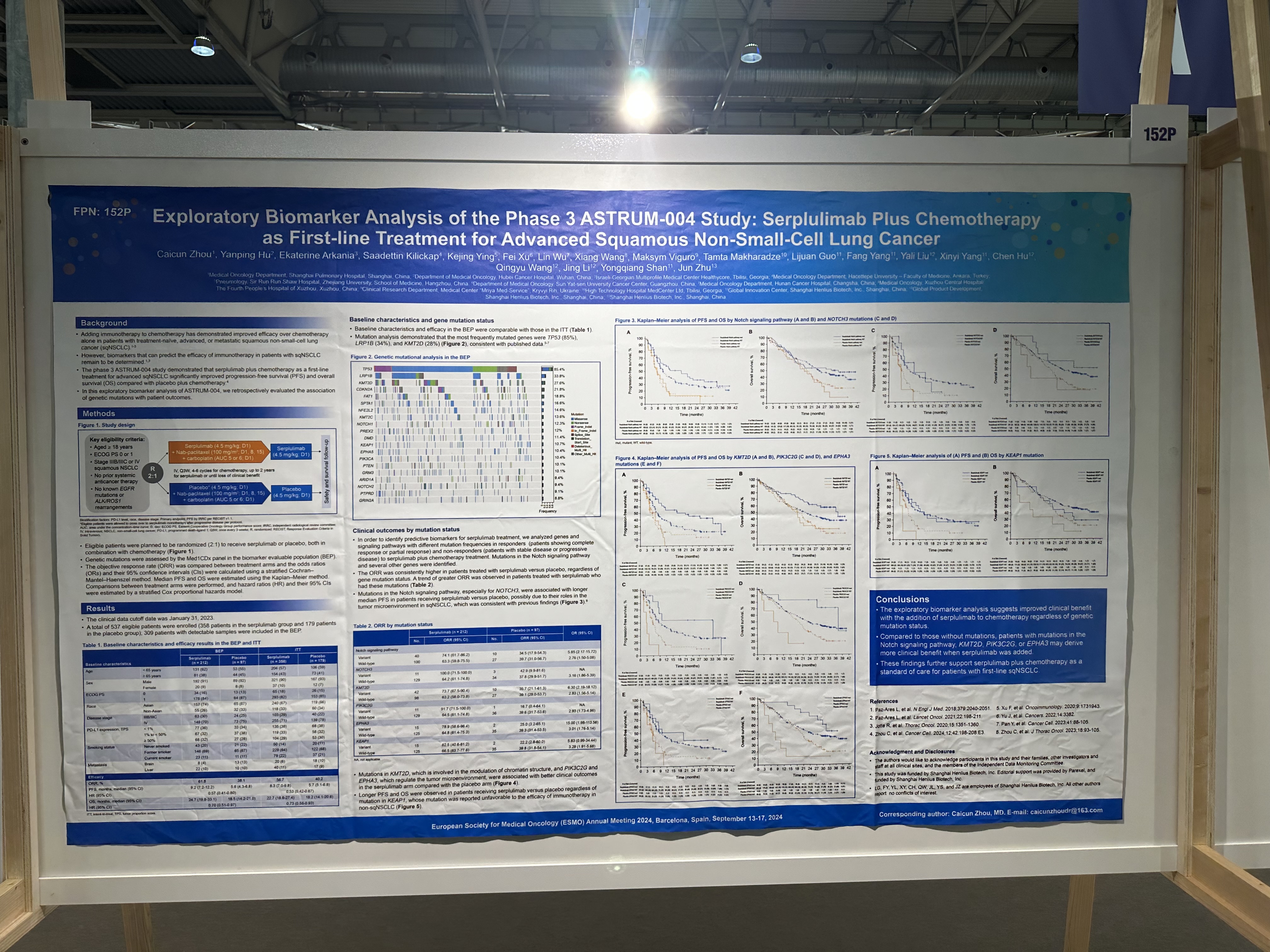
斯魯利單抗聯合化療一線治療鱗狀非小細胞肺癌的關鍵III期臨床研究ASTRUM-004的探索性生物標誌物分析
試驗方法
對符合要求的患者進行隨機分組,按照2:1的比例接受斯魯利單抗或安慰劑治療,兩者均與化療聯合使用。
生物標誌物可評估人群(BEP)樣本經 Med1CDxTM panel進行高通量測序分析基因突變。採用分層 Cochran-Mantel-Haenszel 法比較不同治療組的客觀緩解率(ORR),計算優勢比(OR)及其 95% 置信區間(CI)。採用 Kaplan-Meier 法計算中位 PFS 和 OS。不同治療組之間通過分層 Cox 比例風險回歸模型估計風險比(HR)及其 95% CI。
結果
臨床數據截止日期為 2023 年 1 月 31 日。共有 537 名符合條件的患者入組(斯魯利單抗組358 人,安慰劑組179 人),309 名有可檢測樣本的患者被納入BEP。
基線特徵和基因突變情況
BEP的基線特徵和療效與ITT相當。
基因突變分析表明,最常見的突變基因為TP53(85%)、LRP1B(34%)和 KMT2D(28%),與既往報道的結果一致[8-10]。
突變情況的臨床結果
為確定斯魯利單抗治療的預測性生物標誌物,我們分析了經斯魯利單抗聯合化療治療後,疾病緩解者(完全緩解或部分緩解的患者)和未緩解者(疾病穩定或進展患者)中不同突變頻率的基因和信號通路,發現了Notch信號通路和其他一些基因的突變與斯魯利單抗聯合化療更好的治療效果相關。
無論基因突變情況如何,斯魯利單抗治療組患者的ORR始終高於安慰劑組的患者,存在上述基因突變患者的 ORR 有提高的趨勢
Notch信號通路中的基因突變,尤其是NOTCH3基因突變,與接受斯魯利單抗治療患者的中位無進展生存期(PFS)延長有關。與安慰劑組相比,斯魯利單抗治療組患者的PFS更長,這可能是因為它們在 sqNSCLC腫瘤微環境中發揮作用,這與之前的報道一致[11]。
結論
探索性生物標誌物分析表明,無論基因突變情況如何,在化療中聯合斯魯利單抗都能提高患者的臨床獲益。與沒有基因突變的患者相比,Notch信號通路、KMT2D、PIK3C2G或EPHA3突變的患者可能會在斯魯利單抗治療中取得更高的臨床獲益。這些研究結果進一步支持斯魯利單抗聯合化療作為一線sqNSCLC患者的標準治療方案。
ASTRUM-LC01
論文題目
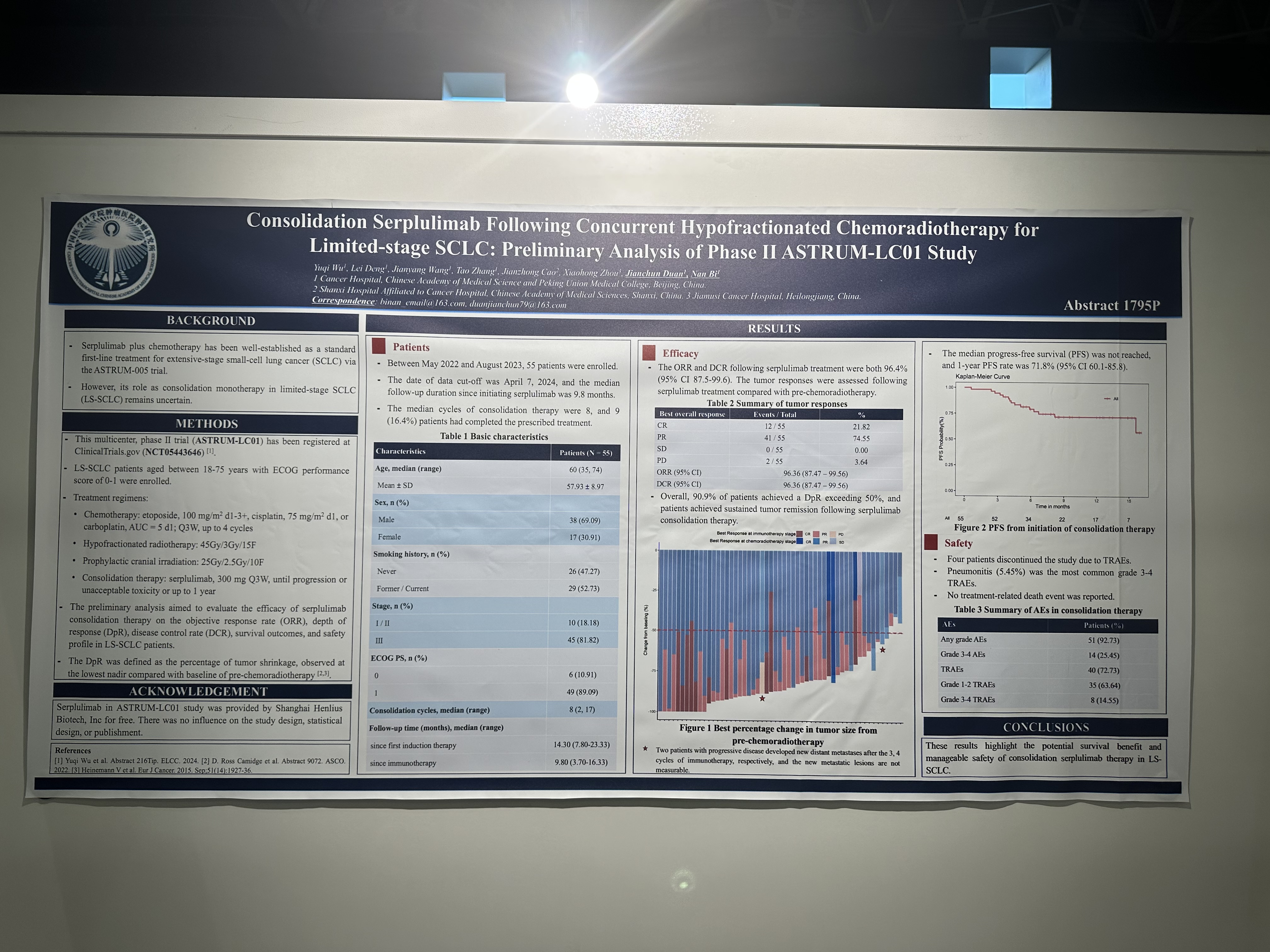
ASTRUM-LC01:同步放化療後斯魯利單抗鞏固治療LS-SCLC
試驗方法
這項多中心、II期臨床試驗(ASTRUM-LC01)納入18~75歲、ECOG PS評分為0-1、接受4個周期標準化療及同步大分割放療(45Gy/3Gy/15F)和預防性顱腦照射(25Gy/2.5Gy/10F)後無進展的LS-SCLC患者,給予患者斯魯利單抗鞏固治療直至疾病進展或不可耐受毒性,治療最長至1年時間,旨在評估斯魯利單抗鞏固治療LS-SCLC患者的客觀緩解率(ORR)、 DpR (腫瘤緩解深度,定義為與誘導期相比腫瘤縮小的比例)、疾病控制率(DCR)、生存結局和安全性。
結果
在2022年5月至2023年8月期間,研究入組55名患者。數據截止日期為2024年4月7日,自開始使用斯魯利單抗起的中位隨訪時間為9.8個月。中位鞏固治療周期數為8個周期,9名(16.4%)患者完成了1年鞏固治療。
療效數據顯示,研究的ORR和DCR均為96.36%(與放化療基線相比),90.9%的患者DpR超過50%,並且在接受斯魯利單抗鞏固治療後,患者實現了持續腫瘤緩解。
研究的整體安全性可控,3-4級的治療相關不良事件(TRAE)發生率為14.55%,其中肺炎(5.45%)是最常見的3-4級TRAE,無治療相關死亡事件發生。
結論
研究結果顯示同步放化療後斯魯利單抗鞏固治療LS-SCLC具有顯著的療效獲益和可控的安全性。
一項回顧性真實世界研究
論文題目
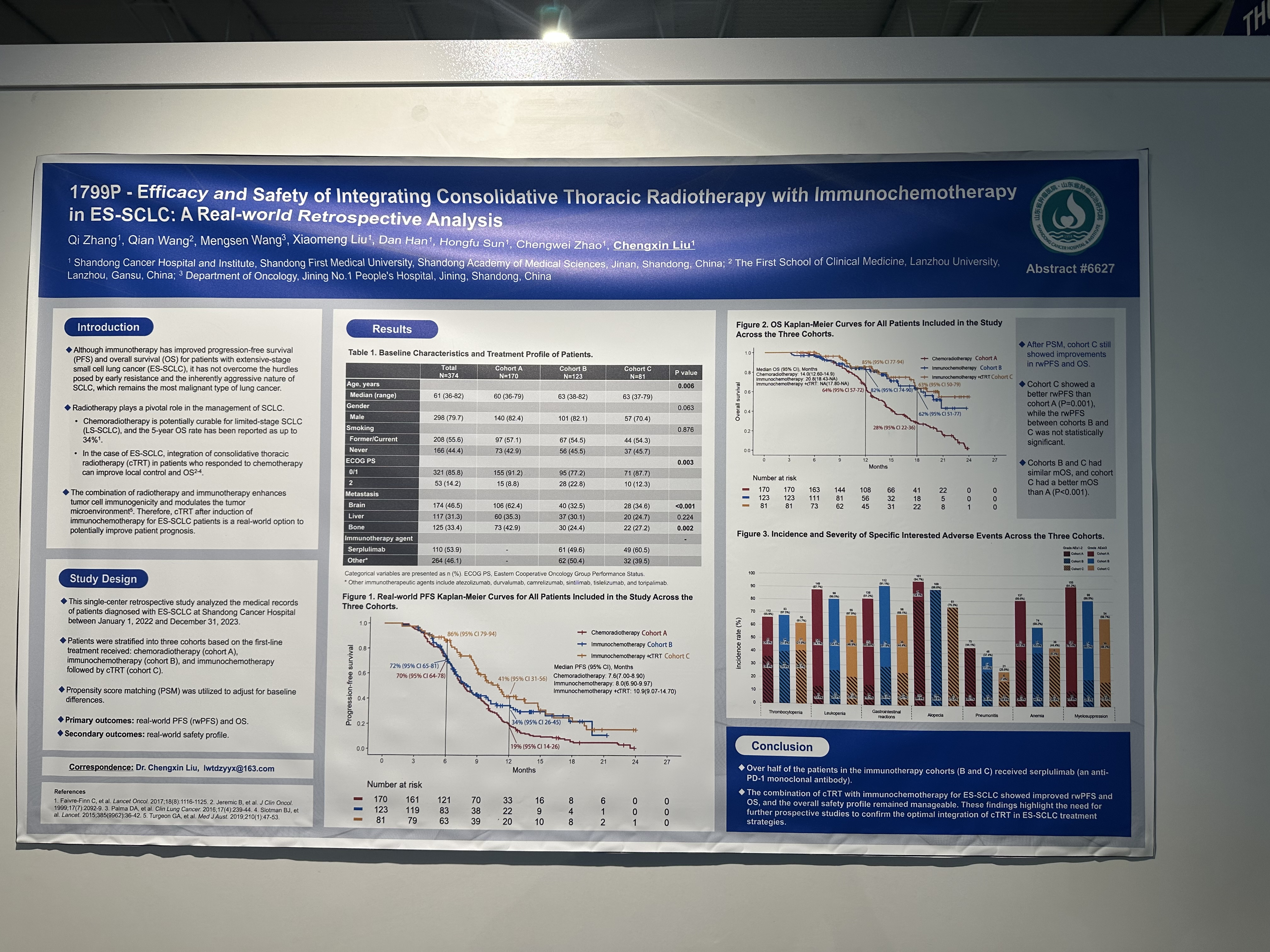
免疫聯合化療及胸部放療治療ES-SCLC的療效和安全性:一項回顧性真實世界研究
研究設計
這項在山東省腫瘤醫院開展的單中心研究,回顧性分析2022年1月1日至2023年12月31日接受治療的828 例 ES-SCLC 患者。根據治療情況,將患者分為放化療組(隊列A) 接受4-6個周期化療後進行胸部放療、免疫化療組(隊列B) 接受4-6周期免疫聯合化療後免疫維持、免疫化療+放療組 (隊列C)接受4-6周期免疫聯合化療後免疫+cTRT維持治療。採用傾向評分匹配(PSM) 調整基線差異。主要研究終點為rwPFS和OS,次要終點為安全性。
結果
納入分析374例患者,接受斯魯利單抗治療的患者110例(53.9%)。療效結果顯示,免疫化療+放療組的rwPFS和OS較放化療組顯著改善,免疫化療+放療組的中位rwPFS優於免疫化療組和放化療組(10.9個月vs 8.0個月 vs 7.6個月),免疫化療+放療組的1年rwPFS率高於免疫化療組和放化療組(41% vs 34% vs 19%),免疫化療+放療組和免疫化療組及放化療組的中位OS分別為NA vs 20.8個月vs 14個月,免疫化療+放療組的18個月OS率高於免疫化療組和放化療組(63% vs 62% vs 28%)。傾向性評分匹配分析結果顯示,相比於放化療組,免疫化療後放療組仍然能夠顯著提升患者的mPFS和mOS。安全性數據表明,≥3級不良事件的發生率在各組間相當,以骨髓抑制最為常見,≥3級肺炎的發生率在免疫化療組和免疫化療+放療組明顯較高,與既往報道一致。
結論
免疫聯合化療序貫胸部放療治療ES-SCLC的rwPFS和OS均有改善,總體安全性可控。未來可進一步開展前瞻性研究以確認在ES-SCLC治療策略中聯合cTRT的最佳方法。
一項開放標籤的單臂II期臨床研究

論文題目
斯魯利單抗聯合化療圍手術期治療可切除的鱗狀非小細胞肺癌患者:一項開放標籤、單臂、II期臨床研究
研究設計
這是一項開放標籤、單臂、II期研究,旨在評估斯魯利單抗圍術期治療可切除鱗狀NSCLC患者的療效。納入18~75歲可手術切除的II-IIIA期鱗狀NSCLC,患者給予斯魯利單抗(300mg)聯合白蛋白紫杉醇和卡鉑新輔助治療2-3個周期,輔助治療為1-2個周期,共4個周期。主要終點是主要病理緩解(MPR),次要終點是病理完全緩解(pCR)。
結果
研究共納入30例患者,IIIA期患者有16例(53.3%),29例患者行手術切除,28例(93.3%)患者達到R0切除(表1)。MPR率為76.7%, pCR率為50%。ORR為73.33%,其中2例(6.67%)患者達到CR(表2)。中性粒細胞減少症(43%)是最常見的3-4級不良事件 (表3)。新輔助治療後循環腫瘤DNA清除率是pCR的重要預測因子(P=0.007),敏感性為78.6%,特異性為76.9%。
結論
斯魯利單抗聯合含鉑化療新輔助和輔助治療是可切除鱗狀NSCLC的一種有希望的治療方法,具有高MPR率和pCR率,安全性可控。
HER2 陽性 II-III 期乳腺癌新輔助治療的 II 期研究
論文題目
吡咯替尼聯合白蛋白紫杉醇及曲妥珠單抗HLX02用於HER2 陽性 II-III 期乳腺癌新輔助治療的 II 期研究
試驗方法
先前未經治療的非轉移性HER2陽性BC患者被分配接受6個新輔助周期,每日一次口服吡咯替尼(400 mg),加HLX02 (8 mg/kg負荷劑量,隨後是6 mg/kg)和nabp (260 mg/m2)。主要終點為pCR (ypT0/isN0)。在基線(P0)、新輔助治療後(P1)和手術後(P2)使用metafer - se - fish全自動CTC圖像掃描與分析系統捕獲和計數CTC,並在BZ-X800顯微鏡採集圖像後使用Imaris 10.1進行分析。
結果
從2020年12月至2023年8月,共有214例患者入組並完成新輔助治療和手術。pCR率為62.96% (95% CI, 55.65% ~ 69.86%,p=.001)。最常見的3-4級不良事件是腹瀉(34.7%)和中性粒細胞減少(6.5%)。在95例接受ctc分析的患者中,63例(66.3%)實現了pCR。與P0組相比,P1組ctc計數明顯減少(3.06±3.38 vs.0.84±1.53 FU/5ml, p< 0.001)。與非pcr組相比, pCR患者在P0時細胞核大小較大(95% CI, 1.02-1.38;P =.04),較少細胞計數(95% CI, 1.49-8.28;P =.03)和較低的膜強度(95% CI,0.93-0.98;P =.03)。
結論
在HER2陽性,II-III期BC的女性中,吡咯替尼+ HLX02和nabp新輔助方案有效地促進了腫瘤的pCR,並呈現出可接受的耐受性。在早期BC的新輔助治療期間對CTC進行個性化監測可能有助於實時評估治療反應並有助於預測pCR。
參考文獻
1. Rizvi H, et al. J Clin Oncol. 2018;36:1645.
2. Song K, et al. Transl Lung Cancer Res. 2018;7:439-449.
3. Mayakonda A, et al. Genome Res. 2018;28:1747-1756.
4. Alexandrov LB, et al. Nature. 2013;500:415-421.
5. Rosenthal R, et al. Genome Biol. 2016;17:31.
6.Zhou H, et al. Nat Commun. 2021;12:5431.
7.George J, et al. Nature. 2015;524:47-53.
8. Xu F, et al. Onomatology. 2020;9:1731943.
9. Yu J, et al. Cancers. 2022;14:3382.
10. Pan Y, et al. Cancer Cell. 2023;41:88-105.
11. Zhou C, et al. J Thorac Oncol. 2023;18:93-105.
