2024年3月14日,復宏漢霖(2696.HK)宣布,基於與宜聯生物的合作,公司開發的EGFR靶向抗體偶聯藥物(antibody-drug-conjugate, ADC)注射用HLX42用於晚期/轉移性實體瘤治療的I期臨床研究(NCT06210815)於中國完成首例受試者給藥。此前,HLX42用於治療晚期/轉移性實體瘤治療的臨床試驗申請已經相繼獲得中國國家藥品監督管理局(NMPA)、美國食品和藥物監督管理局(FDA)許可。2023年12月,HLX42用於治療經第三代EGFR酪氨酸激酶抑制劑治療(TKI)後疾病進展的EGFR突變的晚期/轉移性非小細胞肺癌(NSCLC)獲得FDA快速通道資格認定。
表皮生長因子受體(EGFR)屬於受體酪氨酸激酶,在細胞增殖、分化和遷移的過程中發揮重要作用。研究發現,與正常組織相比,EGFR的突變或者高表達與非小細胞肺癌、結腸癌等腫瘤的發生密切相關,是抗腫瘤藥物開發中的重要靶點[1]。儘管多款EGFR抗體和第三代EGFR TKI已經在腫瘤治療中獲得了廣泛成功,但對於因耐藥而導致的標準治療失敗或治療後復發的腫瘤患者,仍存在未滿足的臨床需求[2]。近年來,隨着ADC技術的快速發展,ADC藥物的開發為腫瘤患者提供了新的治療方案[3],靶向EGFR的ADC藥物有望克服現有靶向EGFR治療的耐藥機制,為更多晚期非小細胞肺癌、結直腸癌等患者帶來臨床獲益。
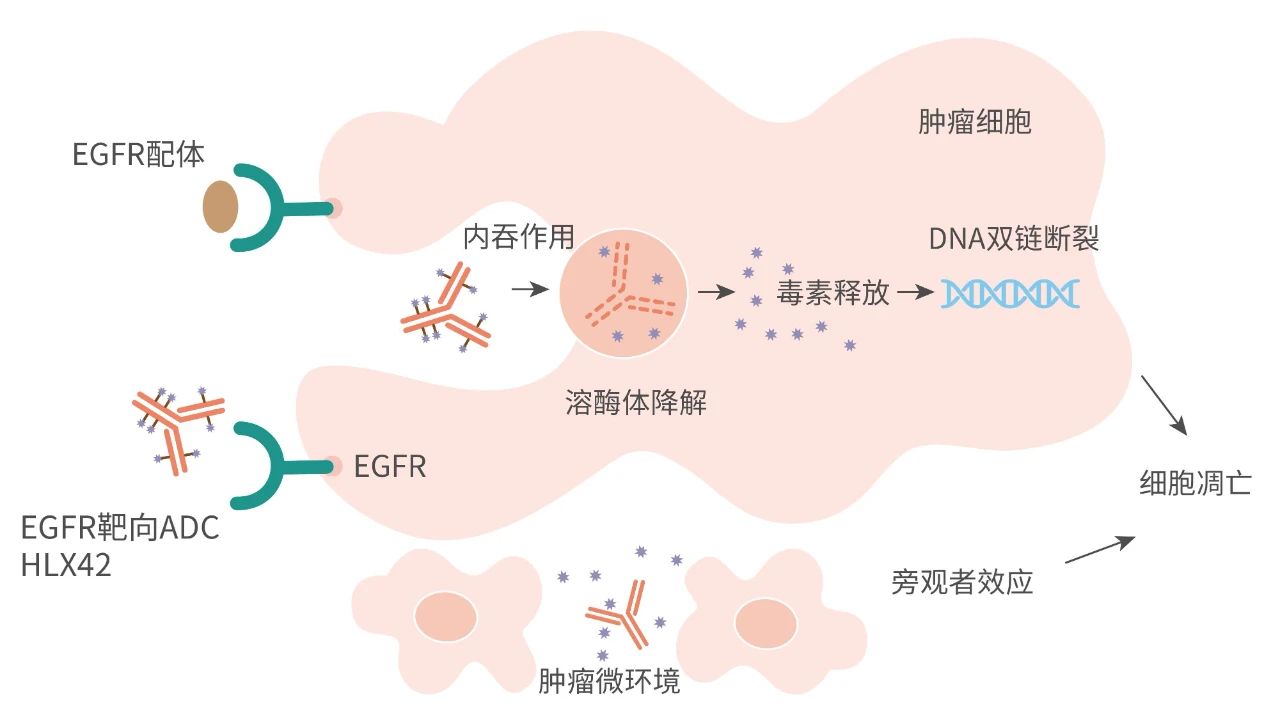
HLX42由高度特異性的人源化lgG1 EGFR抗體分子、可裂解的新型連接子-荷載毒素偶聯製備而成,其藥物抗體比(drug-to-antibody ratio, DAR)約為8。其中,HLX42的荷載毒素為一種新型DNA拓撲異構酶I(Topoisomerase I)小分子抑制劑,通過造成DNA雙鏈斷裂,阻斷DNA複製,從而導致腫瘤細胞凋亡。靜脈輸注後,HLX42的連接子-毒素能夠在腫瘤微環境中特異性裂解釋放,具備較強的旁觀者殺傷效應,獨特的作用機制使得HLX42較同類ADC產品具有更大的治療窗口,增強ADC在實體腫瘤中的治療效果。HLX42在臨床前藥效研究、藥代動力學研究及安全性評價中展現出良好的抗腫瘤活性和安全性,相關數據已於2023歐洲腫瘤內科學會(ESMO)大會以壁報形式首次發布。在第三代EGFR TKI(奧希替尼)或抗EGFR單克隆抗體(西妥昔單抗)耐藥的非小細胞肺癌、結直腸癌等腫瘤模型中,HLX42顯示出良好的腫瘤殺傷效果,有望克服現有靶向EGFR治療的耐藥機制,填補更多晚期/轉移性實體瘤患者未滿足的臨床需求。
復宏漢霖以患者為中心、從臨床需求出發,目前已打造出多元化、高質量的創新產品管線,涵蓋約60個分子,覆蓋單抗、雙抗、ADC、融合蛋白、小分子藥物等藥物形式,其中超過80%的產品為自主開發。未來,公司將繼續以抗體為核心,積極探索新靶點、新機制,不斷拓展產品疾病領域和新分子類型,推動更多創新產品的臨床研究,期待早日為更多患者帶來可負擔的高品質生物藥。
【參考文獻】
[1] Ni cholson, Robert Ian, Julia Margaret Wendy Gee, and Maureen Elaine Harper. EGFR and cancer prognosis. European journal of cancer 37 (2001): 9-15.
[2] Tan, Chee Seng, D. Gilligan, and S. Pacey. Treatment approaches for EGFR-inhibitor-resistant patients with non-small-cell lung cancer. The Lancet Oncology 16.9(2015): e447-59.
[3] Ponziani S, Di Vittorio G, Pitari G, et al. Antibody-Drug Conjugates: The New Frontier of Chemotherapy. Int J Mol Sci. 2020 Jul 31;21(15):5510.
關於NCT06210815
本研究為一項評估HLX42(抗EGFR的抗體偶聯藥物【ADC】)在晚期/轉移性實體瘤患者中的安全性、耐受性的開放、劑量遞增、首次人體Ⅰ期臨床研究。研究將採用「3+3」劑量遞增方法,患者將接受7個不同劑量水平(0.1 mg/kg、0.3 mg/kg、0.6 mg/kg、1.2 mg/kg、2.0 mg/kg、3.0 mg/kg、4.0 mg/kg)的HLX42靜脈輸注給藥,每三周一次。劑量限制性毒性(DLT)觀察期為HLX42首次給藥後的三周。本研究的主要終點為DLT觀察期內每個劑量組發生DLT事件的患者比例,以及HLX42的最大耐受劑量(MTD)。次要終點包含安全性、藥代動力學參數、免疫原性、初步療效、藥效學指標,以及潛在預測性和耐藥性生物標誌物。
