2022年12月2~4日,歐洲腫瘤內科學會亞洲年會(ESMO
ASIA 2022)在新加坡和線上同步召開,來自全球和亞太地區的專家學者齊聚一堂,探討腫瘤領域的最新研究進展,共同為抗擊癌症貢獻力量。
大會首日,中國醫學科學院腫瘤醫院黃鏡教授作為Leading
PI口頭報告了一項食管癌免疫治療的III期臨床研究——ASTRUM-007研究(摘要號:69O,報告時間:12月2日 16:55-17:05)。ASTRUM-007研究由全國70家中心共同參與開展,比較了斯魯利單抗或安慰劑聯合化療一線治療局部晚期/轉移性、PD-L1陽性(CPS≥1)食管鱗癌(ESCC)患者的療效和安全性,結果證明斯魯利單抗可帶來無進展生存期(PFS)、總生存期(OS)的顯著獲益,且CPS評分越高,獲益越大。

黃鏡教授ESMO ASIA 2022線上口頭報告
斯魯利單抗是由我國民族藥企複宏漢霖自主研發的創新性PD-1抑制劑,近年來在腫瘤領域多次創下佳績,現於國際舞臺再次發出中國好聲音,令人振奮。因此,本報特別整理ESMO
ASIA 2022口頭報告內容,並邀請黃鏡教授解讀研究資料,分享研究體會,點評臨床意義。
ASTRUM-007研究現場速遞
研究背景
食管癌是世界上最常見的癌症之一,2020年全球癌症統計報告顯示,食管癌的發病率和死亡率分別列全部惡性腫瘤的第10位元和第6位[1]。亞洲食管癌病例約占全球食管癌病例80%,中國食管癌病例占全球食管癌54%,患者基數龐大[2]。
斯魯利單抗是新型PD-1抑制劑,在多種瘤種中表現出了出色的療效和良好的安全性,已於2022年3月在我國獲批上市,用於治療不可切除或轉移性微衛星高度不穩定(MSI-H)的成人晚期實體瘤經治患者;同年10月,獲批用於一線治療局部晚期或轉移性鱗狀非小細胞肺癌。
研究設計
這是一項隨機、雙盲、多中心、安慰劑對照的III期臨床試驗(NCT03958890)。主要納入標準包括:①年齡為18~75歲,②經組織學確診的不可手術切除或通過放化療治癒的局部晚期/復發或遠處轉移的ESCC,③未接受過針對本次腫瘤的系統性治療,④至少有一個可測量的病灶,⑤PD-L1陽性(CPS≥1),⑥ECOG評分為0或1。患者按照2:1的比例隨機分配至實驗組和對照組,兩組治療方案分別為斯魯利單抗或安慰劑(3
mg/kg,D1)+ 順鉑(50 mg/m2,D1)+ 5-FU(2400 mg/m2,D1-2),每2周1次,順鉑最長治療8個週期,5-FU最長治療12個週期,斯魯利單抗最長治療2年,或直至發生疾病進展、毒性不耐受或其他事件。研究的主要終點為PFS(由獨立影像評估委員會(IRRC)據RECIST v1.1評估)和OS,次要終點包括PFS(由IRRC據iRECIST評估、由研究者據RECIST v1.1和iRECIST評估)、客觀緩解率(ORR)、緩解持續時間(DoR)和安全性等。

圖1:試驗設計
研究結果
共計篩選入組551例患者,斯魯利單抗聯合化療組368例,安慰劑聯合化療組183例,截至2022年4月15日,中位隨訪時間為14.9個月。斯魯利單抗聯合化療組和安慰劑聯合化療組患者的基線分佈具有較好的均衡性(見圖2)。總體人群中,≥65歲的患者比例為46.1%(254/551),男性占比為85.3%(470/551),ECOG評分為1患者比例為73.5%(405/551),86.4%(476/551)的患者存在遠處轉移,1≤CPS<10患者比例為56.3%(310/551),CPS≥10患者比例為43.7%(241/551)。
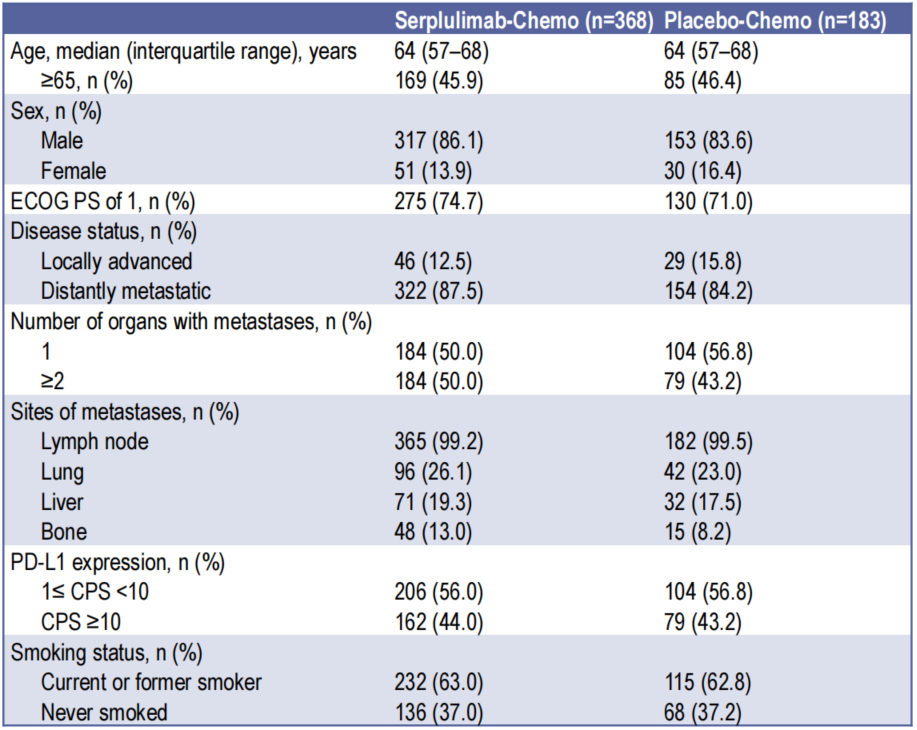
圖2:入組人群基線特徵
主要終點方面,斯魯利單抗聯合化療組的中位PFS(由IRRC據RECIST v1.1評估)和中位OS均較安慰劑聯合化療組顯著延長,CPS≥10人群獲益更大。兩組總人群中位OS分別為15.3m vs 11.8m(HR=0.68,p=0.0020),死亡風險降低32%;CPS≥10人群中位OS分別為18.6m vs 13.9m(HR=0.59,p=0.0082),死亡風險降低41%(見圖3)。兩組總人群中位PFS分別為5.8m vs 5.3m(HR=0.60,p<0.0001),疾病進展風險降低40%;CPS≥10人群中位PFS分別為7.1m vs 5.3m(HR=0.48,p<0.0001),疾病進展風險降低52%(見圖4)。
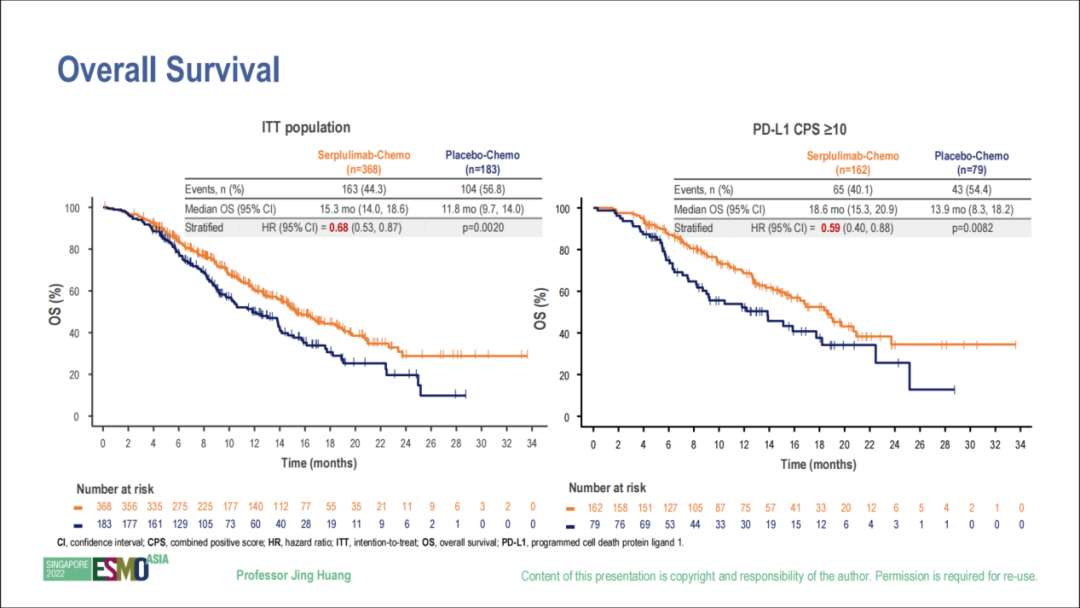
圖3:OS結果
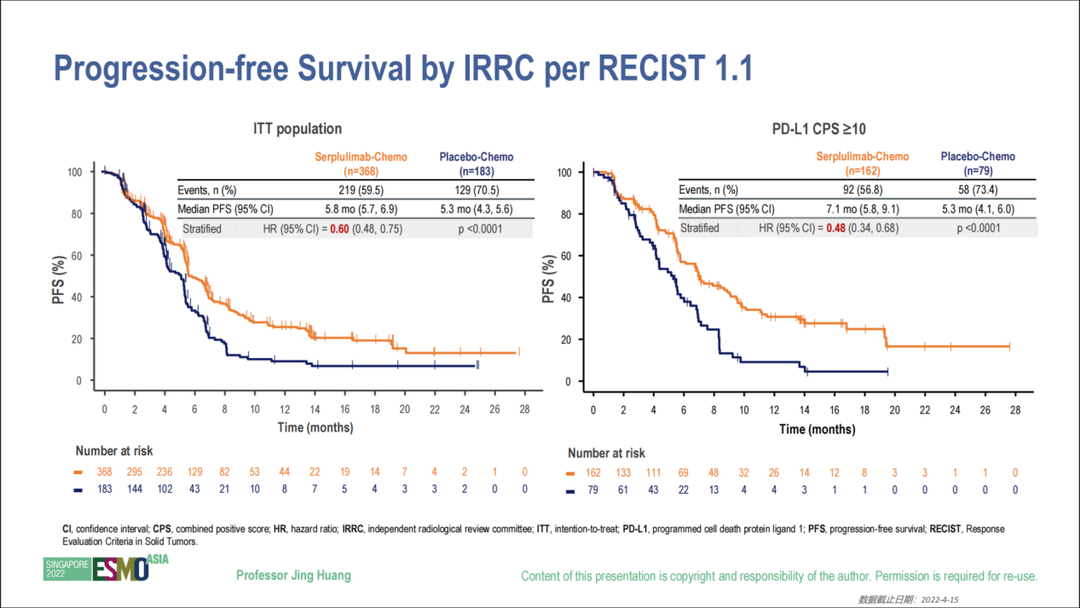
圖4:PFS結果
次要終點方面,斯魯利單抗聯合化療組的ORR較安慰劑聯合化療組顯著改善(圖5)。總人群由獨立影像評估委員會(IRRC)評估,並經過確認的ORR(Confirmed ORR)分別為57.6%(50例完全緩解+162例部分緩解)vs 42.1%(12例完全緩解+65例部分緩解),差異具有統計學意義(p=0.0007);中位DoR分別為6.9m vs 4.6m(HR=0.53,95% CI 0.39-0.75)。
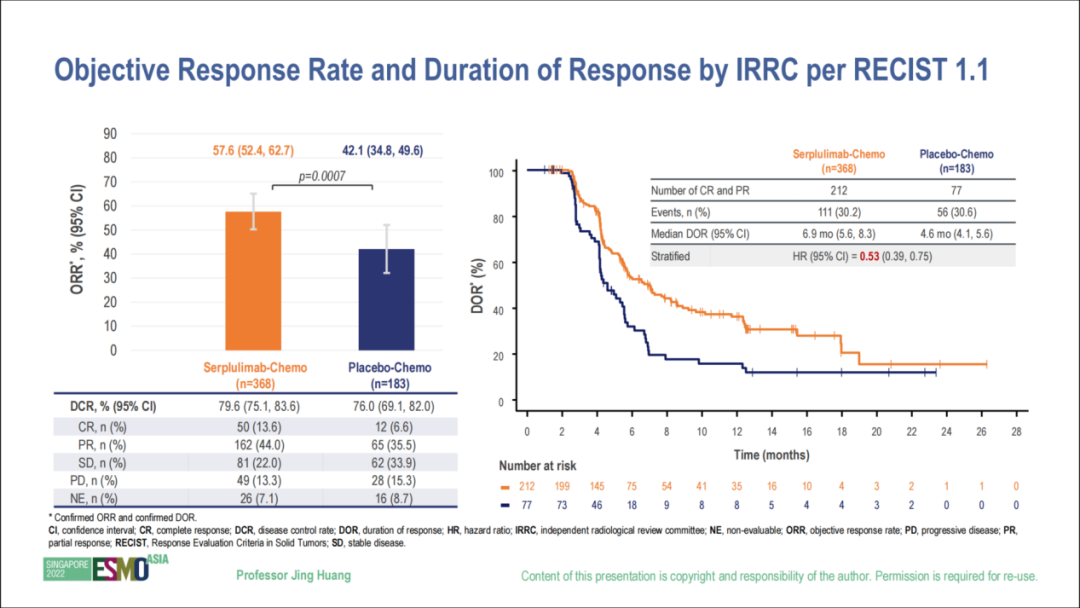
圖5:ORR、DoR結果
安全性方面,斯魯利單抗聯合化療組和安慰劑聯合化療組分別有243(63.6%)及99(58.9%)例患者發生≥3級治療相關不良事件(TRAEs),分別有11(2.9%)和3(1.8%)例患者發生了與治療相關的死亡。斯魯利單抗聯合化療組免疫相關不良事件(irAEs)發生率較安慰劑聯合化療組高(34.6% 和17.9%),與已獲批的PD-1/PD-L1抑制劑相似。最常見的irAEs包括免疫介導性甲狀腺功能減退、免疫介導性皮炎和免疫介導性甲狀腺功能亢進症。見圖6。

圖6:安全性結果
研究結論
試驗結果表明,斯魯利單抗聯合化療(順鉑+5-FU)一線治療局部晚期/轉移性、PD-L1陽性(CPS≥1)食管鱗癌患者具有顯著的療效和良好的安全性,有望為此類患者提供一種新的治療選擇。
斯魯利單抗國際品質
超越典範,精准人群
為更多患者帶來更好生存獲益
黃鏡教授:
我國是食管癌大國,每年的發病和死亡人數約占全球的一半。由於飲食生活習慣的不同,我國食管癌與西方國家有較大區別。一是,中國食管癌的組織學類型以鱗癌為主(90%),而西方國家以腺癌為主[3];二是,中國食管癌主要位於食管中上段,而西方國家多位於食管下段[4,5]。來自歐美的以食管腺癌為主的治療指南無法滿足我國的臨床實踐,因此,開展更多基於中國人群的臨床試驗,豐富我國食管癌的循證醫學證據極為重要。ASTRUM-007研究由全國70家中心共同參與開展,納入了中國551例食管鱗癌患者,貼合中國臨床實踐,其得出的結論對於中國臨床具有重要的指導意義。
手術和放化療是既往進展期食管鱗癌的主要治療手段,但整體療效不佳,臨床上迫切地需要新的治療手段來提高食管癌患者治療療效、改善其預後。免疫治療的出現打破了該治療窘境,食管癌的研究和臨床實踐都進入了免疫治療時代,患者的預後得到實質性改善。
研究設計上,ASTRUM-007試驗有兩大不同之處,一是化療方案的週期選用了雙周重複的方案,比其他幾項研究的給藥頻率更為密集,這主要是基於密集化療可能優於常規化療的考慮,其他瘤種的研究顯示劑量密集化療比常規化療具有更好的療效(圖7)。其二,ASTRUM-007研究從篩選可能有效人群的角度,選擇了CPS≥1的患者參加ASTRUM-007研究。KEYNOTE-590和ORIENT-15研究均提示患者CPS評分越高,免疫治療獲益越大。
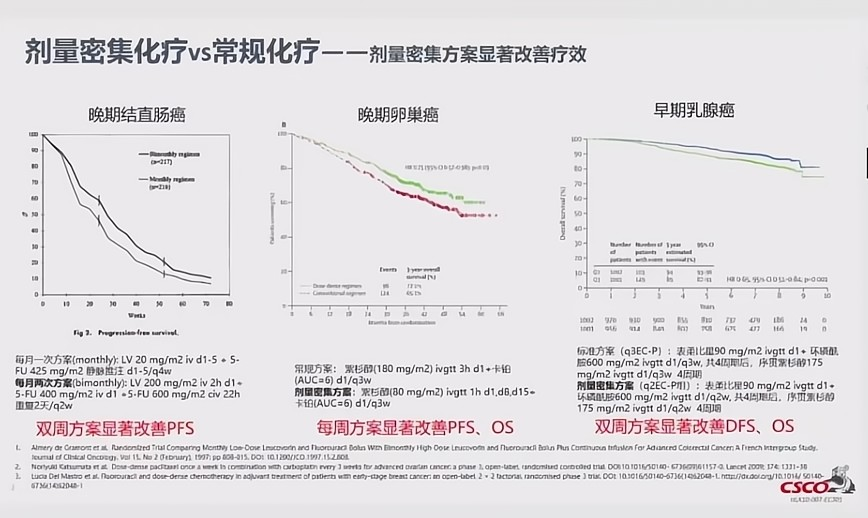
圖7:密集化療對比常規化療
療效獲益上,ASTRUM-007研究充分確證了斯魯利單抗聯合順鉑+5-FU一線治療局部晚期/轉移性、PD-L1陽性(CPS≥1)ESCC患者帶來OS、PFS、ORR和DOR的全面獲益,高有效率轉化為了長期生存改善。不同研究的入組人群都不同,並不能直接對比,但從目前的資料來看,ASTRUM-007研究的斯魯利單抗聯合順鉑+5-FU方案毫不遜色。例如,在CPS≥10的人群,Checkmate-648研究中實驗組和對照組中位OS為16.1m vs 11.6m(HR=0.63)[6],ORIENT-15研究中為17.2m vs 13.6個月(HR=0.64)[7],而ASTRUM-007研究中為18.6m vs 13.9m(HR=0.59),中位OS獲益更長,患者死亡風險降低更多。安全性方面,ASTRUM-007研究顯示斯魯利單抗聯合順鉑+5-FU方案安全性可控,研究期間未觀察到新的安全信號。
ASTRUM-007研究凝聚了眾多研究者和強大藥企團隊的智慧與付出,全國70家臨床中心共同參與,這一成果能夠亮相於2022
ESMO ASIA,實在振奮人心。在此,我們衷心感謝受試者及其家屬對本研究、對食管癌領域發展的支持與貢獻。基於ASTRUM-007研究,斯魯利單抗聯合化療一線治療局部晚期/轉移性食管鱗癌的上市註冊申請已獲得中國國家藥品監督管理局(NMPA)的受理,期待斯魯利單抗一線治療食管癌的適應症能夠早日獲批,惠及更多患者。
參考文獻:
1.Sung
H, et al. Global Cancer Statistics 2020. CA Cancer J Clin. 2021;71(3):209-249.
2.Global Cancer Observatory. International Agency for Research on
Cancer. https://gco.iarc.fr/. Accessed 24 Oct 2022.
3.文龍, 張彬. 食管癌的治療現狀及趨勢分析[J]. 醫學資訊, 2022, 35(18):4.
4.Fujita Hiromasa,Ways and tradition of Japan in esophageal surgery for
cancer.[J] .Gen Thorac Cardiovasc Surg, 2020, 68: 1187-1192.
5.毛友生,高樹庚,王群,等.中國食管癌臨床流行特徵及外科治療概況大資料分析[J].中華腫瘤雜誌,2020,42(3):228-233.
6.Doki Y, Ajani JA, Kato K, et al. Nivolumab Combination Therapy in
Advanced Esophageal Squamous-Cell Carcinoma. N Engl J Med. 2022;386(5):449-462.
7.Lu Zhihao,Wang Junye,Shu Yongqian et al. Sintilimab versus placebo in
combination with chemotherapy as first line treatment for locally advanced or
metastatic oesophageal squamous cell carcinoma (ORIENT-15): multicentre,
randomised, double blind, phase 3 trial.[J] .BMJ, 2022, 377: e068714.
